هموروئید یا بواسیر
هموروئید یا بواسیر
هِموروئید یا بواسیر بیماری مزمن و شایعی است که اکثر انسان های بالغ در دورهای از زندگی به آن دچار می شوند. این عارضه با خارش و احساس ناراحتی و شاید خون ریزی همراه است(1). هِموروئید عبارت است از سیاهرگهای گشاد شده و واریسی در مقعد که ممکن است در مجرای مقعدی (بواسیر داخلی یا خارجی ) ایجاد شود. این عارضه میتواند به هنگام دفع مدفوع درد و ناراحتی و گاهی خون ریزی به همراه داشته باشد.(2). میزان بروز هِموروئید به طور متوسط 36/4% است و هر سن و جنسی را درگیر می کند و بروز آن معمولاً بین سنین 65-45 سال است. هِموروئید ناشی از گرفتاری سیاهرگهای ناحیه مقعدی هستند(1). اگر به هر علتی، فشار بیش از حد به پایین راست روده (رکتوم) و ناحیه مقعدی وارد شود، بهطور غیرطبیعی این سیاهرگها متورم میشوند. فشار زیاد، ممکن است به علت وارد آمدن فشار مکرر به سیاهرگهای مقعد یا راست روده عوامل افزایش دهنده خطر، رژیم غذایی بدون فیبر، نشستن یا ایستادن به مدت طولانی، چاقی، یبوست، مواجهه با ارتعاش در محیط های كاری (مانند رانندگان لیفتراك یا محیط های مرتعش مانند ژنراتورهای نیروگاه ها) کمشدن توان عضلانی در سنین بالا، جراحی راست روده، بیماری کبدی، سرطان روده بزرگ بالا بردن فشار خون در سیستم سیاهرگی دستگاه گوارش باشد(2).
انواع هِموروئید
هِموروئید خارجی: در این حالت هِموروئید از درون روده متورم می شود و بیمار درد و ناراحتی بسیاری دارد و در هنگام دفع مدفوع منجر به خون ریزی می گردد.
هِموروئید داخلی: این نوع هِموروئید یا بواسیر در زیر پوست کنار مقعدایجاد میشود. در این نوع هِموروئید بسیار حساس تر است و بیمار احساس درد وخارش بیشتری دارد.
هِموروئید ترومپوز:این نوع بسیار دردناک تر است و بیمار هر چند ساعت یک بار با علائم هِموروئید روبرو میشود.
علائم و نشانه های بروز هِموروئید خونریزی، درد حین اجابت مزاج، خارش، ترشح موکوسی ، توده و التهاب در ناحیه مقعد می باشد(3). درمان بیماران شامل درمان های حمایتی، مداخله غیربرشی هموروئید rubber band ligation، اسکلروتراپی، فوتوکواگولاسیون، کرایوتراپی و در نهایت excision همورئید است. از عوارض مهم بعد از عمل جراحی هِموروئید می توان به درد، خونریزی، تنگی آنال، بی اختیاری در دفع گاز و احتباس ادراری اشاره کرد(4).
بیمارى هموروئید را بر اساس شدت و وسعت اختلالى که عروق سیاهرگى درون مقعد ایجاد کرده و همچنین میزان برون زدگى مى توان به 4 درجه تقسیم کرد.
درجه 1: در مرحله ابتدایى بیمارى هموروئید فقط شامل تورم عروق سیاهرگى درون راست روده است، بسته به شدت ورم و تجمع خون در آنها ممکن است در مواقعى که تحت فشار قرار مى گیرند به صورت قطره اى خون ریزى کنند.
درجه 2: در مرحله دوم پیشرفت بیمارى هموروئید داخلى در صورتى که فرد با دقت باشد ممکن است متوجه برآمدگى ناحیه مقعد به اندازه یک نخود در هنگام اجابت مزاج شود که پس از دفع مدفوع خود به خود از بین رفته و درون مقعد باز مى گردد.
درجه 3: در سومین مرحله بیمارى، دیگر توده گوشتى ایجاد شده بر روى مقعد قادر به بازگشت خود به خودى درون کانال نخواهد بود ولى فرد قادر است پس از اجابت مزاج هنگام شستشوى خود آن را به کمک انگشت به درون مقعد بازگرداند.
درجه 4: در چهارمین مرحله بیمارى، توده گوشتى ایجاد شده بر روى مقعد دیگر قابل درمان نیست و مى بایست مورد جراحى قرار گیرد(5).
علتهای شایع بروز هِموروئید یا بواسیر:
- رژیم غذایی کم فیبر
- یبوست مزمن
- استرس و فشارهای عصبی
- بالا رفتن فشار خون در سیستم گوارشی
- عارضه های کبدی (مانند سیروز کبدی)
هِموروئید چه عواقب و مشکلاتی می تواند داشته باشد؟
در صورت عدم درمان به موقع هِموروئید می تواند دوباره ظاهر شود. این عارضه می تواند به صورت هِموروئید خارجی، ترومپوز(بسیار دردناک)، هموروید داخلی، خونریزی، یبوست و احتناق بافت مقعدی ظاهر شود.
فرآورده رکتول حاوى اسانس مورت جایگزینى مناسب و ممتاز براى آنتى هموروئیدهاى شیمیایى موجود در بازار است. این فرآورده با بسته بندى مناسب و کامل در دسترس عموم قرار دارد. از جمله خواص بى نظیر رکتول به شرح ذیل مى باشد:
- بى حس کننده موضعى براى درمان علامتى
- برطرف کردن عوارض بیمارى (التهاب و خونریزى)
- ضد قارچ
- ضد باکترى
- لوبریکنت و تسهیل کننده دفع مدفوع این خواص مجموعاً در برگیرنده درمان اغلب عوامل و عوارض بیمارىهاى هموروئید است.
بسته دارویى رکتول حاوى تجهیزات منحصر بفردى شامل (اپلیکاتور به تعداد لازم ،گاز نخى و قطعه تخلیه کننده منظم و کامل تیوب) جهت تسهیل استفاده، نظافت و تکمیل دوز درمانى مى باشد. دارو فاقد هر گونه مواد محرك و شیمیایى است.
مورد درختچه همیشه سبزی است که از خانواده Myrtaceae می باشد و در مناطق مدیترانه ای می روید. مورد گیاهی معطر و خوشبو است و این به دلیل وجود غده های حاوی اسانس در برگ، میوه و گل های آن است. این گیاه از گذشته به دلیل خواص ضدالتهابی، ضد ویروسی، ضدعفونی کنندگی و گندزدایی بسیار مورد توجه قرار گرفته است. بخش دارویی این گیاه را برگها تشکیل می دهند(6). برگ های مورد دارای 5/1 تا 2 درصد حجمی اسانس است. ترکیبات شیمیایی اسانس موردشامل α-پینن، لیمونن، سینئول، لینالول، -αترپینئول، کاریوفیلین می باشد(6).
تقریباً در تمام منابع مستقیم و غیرمستقیم به اثرات آنتى سپتیک، قابض و ضد التهاب گیاه مورت سبز اشاره شده است. اغلب اثرات دارویى مورد ادعاى محققان گذشته و حال پیرامون همین خواص بوده است. علاوه بر این در پژوهشى که به مقایسه اثر اسانس مورت سبز با آنتى هموروئیدهاى موجود در بازار علیه درمان بیمارى هموروئید انجام شد و در خلوص هاى 5/2 و 5 و 10 مورد بررسى قرار گرفت نتایج نشان داد که اسانس مورت سبز با غلظت 5 درصد بیشترین تأثیر را در درمان هموروئید دارد و در مقایسه با آنتى هموروئیدهاى موجود در بازار هم از نظر بیمار و هم از نظر پزشک مورد رضایتمندى قرار گرفته است. آنالیز یافته هاى بالینى نشان مى دهد که فرمول رکتول در مقایسه با پماد شیمیایى که شاهد مثبت تحقیقات رکتول بوده است تأثیر درمانى به مراتب بهترى اعمال کرده است.
توکسیکولوژى: در مطالعات توکسیکولوژى میرتول (ماده مؤثره رکتول) به شکل خوراکى 1 تا 2 میلی لیتر در روز هیچگونه عوارض ناخواسته اى براى انسان ایجاد نکرده است.
تحقیقات بالینى: رکتول بر روى 40 بیمار مبتلا به هموروئید مورد بررسى قرار گرفت که از نظر آمارى اختلاف معنادارى در مقایسه با داروى آنتى هموروئید به نفع رکتول مشاهده گردید. علائم بیمارى شامل درد، خونریزى، خارش و التهاب به شرح ذیل کاهش یافت و قابل مشاهده است. در اکثر موارد پاسخ خوب و عالى در کاهش درد، التهاب، خونریزى و خارش به دست آمده و با استفاده از رکتول ضمن کاهش علائم بهبود و کم شدن درجات بیمارى نیز حاصل شده است. از ویژگى هاى خاص این دارو تسکین فورى درد بیماران است که بلافاصله پس از مصرف ایجاد مى شود. اغلب بیماران از مصرف رکتول ابراز رضایت نموده اند که از این میزان 75درصد رضایت کامل و 25درصد رضایت نسبى نشان داده اند. اما در مورد شاهد، وضعیت به شکل دیگرى است که 25 درصد موارد عدم رضایت و در 75 درصد موارد رضایت وجود داشته که از این تعداد 45 درصد رضایت نسبى و تنها 30 درصد رضایت کامل مشاهده شده است. دقت فرمائید در مقایسه با میانگین 75 درصد رضایت کامل از رکتول، اختلاف معنادارى وجود دارد شکل 1.

شکل 1: نتایج مطالعه بالینی رکتول در 40 بیمار مبتلا به هموروئید

نمودار 2: سیتوتوکسیتی α-pinene در سلولهای ماکروفاژ حفره صفاقی موش که با غلظتهای مختلف α-pinene(0.2-20) به مدت یک ساعت و سپس با (200ng/ml)LPS به مدت 24 ساعت تیمار شد. قدرت زنده ماندن سلول ها با استفاده MTT assay مورد ارزیابی قرار گرفت. α-پینن تا 20میکرومولار هیچگونه اثر سیتوتوکسیک نشان نمی دهد(7).
اثرات ضدالتهابی رکتول
مطالعات متعدد، خواص ضدالتهابی اسانس گیاه مورد M. communis L را در مدل های حیوانی نشان داده اند. اجزاء اصلی اسانس مورد سبز، شامل α-پینن، 1و8- سینئولن، دارای فعالیت ضدالتهابی بصورت سینرژیسم می باشند. α-پینن قویترین اثر ضدالتهابی را از خود نشان می دهد. در این بررسی استفاده موضعی از اسانس مورد سبز باعث کاهش قابل توجهی در ادم گوش و گرانولوم شد. مطالعات نشان داد α-پینن در ماست سل های حفره صفاقی رت آزادسازی هیستامین را مهار می کند(8).
گزارش شده α-پینن IKK-B، NF-kB و کاسپاز-1 را در ماست سل های انسانی فعال می کند. تحقیقات متعدد منجر به این نتیجه گیری می شود که اثرات ضدالتهابی قوی مورد یک رویکرد امیدوار کننده جدید در درمان التهاب حاد است. به طوری که در اثر استفاده مناسب از دوزهای مشخص شده درمانی، هیچگونه خطرات بهداشتی یا عوارض جانبی گزارش نشده است(8).

شکل 2: مهار مسیر MAPK/NF-ƙB[1] در واکنش های التهابی نقش کلیدی در سرکوب مدیاتورهای مهم پیش التهابی NO، [2]PGE2، [3]IL-6 و [4]TNF-α دارد. α-پینن از طریق مهار فسفریلاسیون MAPKs[5] و کاهش بیان [6]IKK خاصیت ضدالتهابی خود را اعمال می نماید.
اثر α-پینن روی مسیر MAPKs/NF-ƙB
فعالیت مسیر MAPKs/NF-ƙB نقش کلیدی در واکنش های التهابی دارد. این مسیر باعث تولید PGE2، NO، IL-6 و TNF-α از مهمترین مدیاتورهای پیش التهابی می شود. α-پینن از طریق سرکوب فعالیت MAPKs و مسیر NF-ƙB خاصیت ضدالتهابی خود را اعمال می نماید. با تحریک LPS، فسفریلاسیون پروتئین های MAPKs شامل ERK و JNK و P38 باعث به راه انداختن واکنش التهابی می شود. فعال شدن این پروتئین ها منجر به رونویسی از ژنهای سیتوکین های پیش التهابی می شود. پروتئین P38 باعث به راه انداختن واکنش های التهابی می شود. فعال شدن این پروتئین ها منجر به رونویسی از ژن های سیتوکین های پیش التهابی می شود. P38 فعال شده منجر به رونویسی ژن های TNF-α و NO از طریق NF-ƙb شده و JNK از طریق فسفوریلاسیون c-Jun و AP-1 اعمال اثر می کند. ERK در تنظیم فعالیت IKK نقش اساسی دارد(7, 9).
در حالت غیر التهاب، پروتئین(IKB) با پروتئین NF-ƙB باند بوده و باعث غیرفعال شدن NF-ƙB می شود. با تحریک LPS پروتئین IKK فسفریله باعث فسفریلاسیون IKB و تجزیه آن شده که این منجر به آزادسازی NF-ƙB می شود. NF-ƙB باعث رونویسی از ژن های واسطه های پیش التهابی شامل iNOS، COX-2، IL-6 و TNF-α می شود. ژن iNOS باعث تولید NO و ژن COX-2 تولید کننده PGE2 می باشد. ملکول NO در اعمال فیزیولوژیکی متنوعی از قبیل التهاب و ارتباطات سلولی دخالت دارد. IL-6 و TNF-α در پاسخ های التهابی که در ارتباط با بیماری های التهابی هستند، نقش اساسی دارند. α-پینن با مهار فسفریلاسیون MAPKs شامل ERK و JNK باعث مهار این آنزیم ها شده و در نتیجه باعث سرکوب آنها می شود. همچنین α-پینن باعث کاهش سطح IKK و در نتیجه کاهش IKB فسفریله و در نتیجه کاهش NF-ƙB می شود(7, 9).

نمودار3: α-پینن تولید IL-6 و TNF-a را در ماکروفاژهای تحریک شده با LPS کاهش می دهد. سلول ها با غلظت های مختلف α-پینن (0.2-20µM) به مدت یک ساعت و سپس با (ng/ml200) LPS به مدت 24 ساعت تیمار شدند. غلظت های(A) IL-6 و (B) TNF-α در سوپرناتانت با استفاده از الایزا اندازگیری شد. تحریک LPS به طور قابل توجهی IL-6 و TNF-α را افزایش می دهد. اما α-پینن تولید آنها در ماکروفاژها را کاهش می دهد. این امر نشان دهنده اثرات ضدالتهابی α-pinene است(7).
اثر مهاری α-پینن روی NO، PGE2، iNOS و COX-2

نمودار 4: α-پینن تولید NO و بیان iNOS در ماکروفاژهای تحریک شده با LPS را مهار می کند. سلول ها با غلظت های مختلف (µM20-2/0) α-پینن به مدت یک ساعت و سپس با (ng/ml200) LPS به مدت 48 ساعت تیمار شدند میزان تولید NO با Griess assay شنجیده شد. α-پینن باعث کاهش NO از طریق کاهش بیان پروتئین iNOS در ماکروفاژها می شود(7).
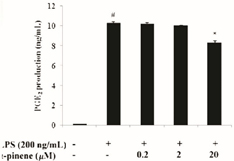
نمودار 5: α-پینن تولید PGE2 و بیانCOX-2 در ماکروفاژهای تحریک شده با LPS را مهار می کند. سلولها با غلظت های مختلف (µM20-2/0) αپینن به مدت یک ساعت و سپس با (ng/ml200) LPS به مدت 24 ساعت تیمار شدند میزان تولید PGE2 از طریق مهار COX-2 در ماکروفاژهای تحریک شده با LPS سنجیده می شود(7).
گزارش شده است که 1 و 8 سینئول، متابولیسم آراشیدونیک اسید و تولید سیتوکین را در مونوسیت های انسانی مهار می کند. مهار مسیر سیکلواکسیژناز به عنوان اولین شاهد از فعالیت بالقوه ضد التهابی 1و 8 سینئول گزارش شده است.
مکانیسم ضدمیکروبی
گفته می شود مکانیسم ضدباکتریایی به دلیل تنها یک مکانیسم نیست. به طور معمول چندین مکانیسم برای فعالیت ضدمیکروبی بیان شده است:
1: فروپاشی غشای سیتوپلاسمی
2- عمل بر روی پروتئین های غشاء مثل ATPase
3- تخریب غشای خارجی باکتری های گرم منفی با آزادسازی لیپوپلی ساکاریدها
4- ناپایداری نیرو محرکه پروتونی
5- مهار سنتز آنزیم ها
فعالیت ضد میکروبی عمدتاً روی غشاء و دیواره ی سلولی اعمال می شود. مطالعات نشان می دهد که نفوذپذیری دیواره و غشای سلولی در حضور اسانس افزایش یافته و منجر به آزادسازی محتوای درون سلولی می شود که این امر می تواند باعث اختلال در عملکرد غشاء نظیر نقل و انتقالات الکترون، فعالیت آنزیم ها و جذب مواد غذایی شود(10، 11 و 12).
فعالیت ضدقارچی اسانس مورد علیه گونه های کاندیدا آلبیکانس نیز سنجیده شده و MIC آن محاسبه شد. گفته می شود فعالیت ضدقارچی اسانس باعث تخریب غشا، نشتی غشای سلولی و در نهایت مرگ سلولی می شود(13).

شکل 3: مکانیسم تاثیر α- پینن بر دیواره باکتری ها
کولووت نوشیدنى آماده تخم ریحان است. این فرآورده داراي موسیلاژ بوده که باجذب آب و نگهداري آن در لوله گوارش موجب حفظ آب در روده و مرطوب ماندن آن و نهایتا جلوگیري از یبوست، نفخ شکم و سبب آرامش و صحت عمومی بدن می گردد. کولووت با حفظ آب جذب شده درفرآیند گوارش سبب نرم شدن مدفوع و نهایتاً بدون تغییر به همراه آب جذب شده از روده خارج و سبب رفع یبوست وعوارض متعاقب آن می گردد. بامصرف کولووت تمام عوارض یبوست اعم از سردرد، عصبانیت، نفخ و صداي روده ها و ازجمله بواسیر رفع می گردند. کولووت با حفظ آب در تمامى مسیر گوارش موجب رفع عطش و تشنگى مخصوصا در فصول گرم سال مى گردد. با مصرف کولووت بخاطر حفظ حجم روده ها از احساس گرسنگى ممانعت می شود. به عبارتى میل به خوردن غذا کمتر مى شود. این امر در فرآیند کاهش وزن و مهار کبد چرب فوق العاده مؤثر است. براى کاهش اشتها 10 دقیقه قبل از غذا یک لیوان نوشیدنى کولووت مصرف گردد
منابع
1. Gentile M, De Rosa M, Carbone G, Pilone V, Mosella F, Forestieri P. LigaSure haemorrhoidectomy versus conventional diathermy for IV-degree haemorrhoids: is it the treatment of choice? A randomized, clinical trial. International Scholarly Research Notices. 2011;2011.
2. Chen J-S, You J-F. Current status of surgical treatment for hemorrhoids-systematic review and meta-analysis. Chang Gung Med J. 2010;33(5):488-500.
3. Panahi Y, Mousavi-Nayeeni SM, Sahebkar A, Fanaie SA, Rahimnia A, Beiraghdar F. Myrtus communis essential oil for the treatment of hemorrhoids: a randomized double-blind double-dummy parallel-group comparative study. Turk J Pharm Sci. 2014;11(1):1-8.
4. Mastakov M, Buettner P, Ho Y-H. Updated meta-analysis of randomized controlled trials comparing conventional excisional haemorrhoidectomy with LigaSure for haemorrhoids. Techniques in coloproctology. 2008;12(3):229.
5. Aslani A, Emami S, Ghannadi A, Ajdari M. Formulation and physicochemical evaluation of an herbal antihemorrohid ointment from Quercus, Black cumin and Fenugreek for the treatment of internal anal hemorrhoids. J Pharm Sci Tabriz Univ Med Sci. 2009;14:247-57.
6. Ziaei Hezarjaribi H, Dalimi A, Ghasemi M, Ghafari R, Esmaeili S, Armat S, et al. Prevalence of common sexually transmitted diseases among women referring for pap smear in Sari, Iran. Journal of Mazandaran University of Medical Sciences. 2013;22(1):19-24.
7. Kim D-S, Lee H-J, Jeon Y-D, Han Y-H, Kee J-Y, Kim H-J, et al. Alpha-pinene exhibits anti-inflammatory activity through the suppression of MAPKs and the NF-κB pathway in mouse peritoneal macrophages. The American journal of Chinese medicine. 2015;43(04):731-42.
8. Hegazy M-EF, Hamed AR, Mohamed TA, Debbab A, Nakamura S, Matsuda H, et al. Anti-inflammatory sesquiterpenes from the medicinal herb Tanacetum sinaicum. RSC Advances. 2015;5(56):44895-901.
9. Celikel N, Kavas G. Antimicrobial properties of some essential oils against some pathogenic microorganisms. Czech Journal of Food Sciences-UZPI (Czech Republic). 2008.
10. Amensour M, Bouhdid S, Fernández-López J, Idaomar M, Senhaji NS, Abrini J. Antibacterial activity of extracts of Myrtus communis against food-borne pathogenic and spoilage bacteria. International Journal of Food Properties. 2010;13(6):1215-24.
11. Cox S, Mann C, Markham J. Interactions between components of the essential oil of Melaleuca alternifolia. Journal of Applied Microbiology. 2001;91(3):492-7.
12. Hammer KA, Carson CF, Dunstan JA, Hale J, Lehmann H, Robinson CJ, et al. Antimicrobial and anti‐inflammatory activity of five Taxandria fragrans oils in vitro. Microbiology and immunology. 2008;52(11):522-30.
13. Cannas S, Molicotti P, Ruggeri M, Cubeddu M, Sanguinetti M, Marongiu B, et al. Antimycotic activity of Myrtus communis L. towards Candida spp. from clinical isolates. The Journal of Infection in Developing Countries. 2013;7(03):295-8.
[1] Nuclear Factor-Kappa B
[1] Prostaglandin E2
[1] Interleukin-6
[1] Tumor Necrosis Factor-α
[1] Mitogen-activated protein Kinases
[1] Inhibitory protein I kappa β Kinase


